Das Mysterium des "Pankreasschmerzes": Von der Antike in die Zukunft
←
→
Transkription von Seiteninhalten
Wenn Ihr Browser die Seite nicht korrekt rendert, bitte, lesen Sie den Inhalt der Seite unten
Das Mysterium des “Pankreasschmerzes”: Von der Antike in die Zukunft
Die Bauchspeicheldrüse (Pankreas) ist sicherlich eines der außerordentlichsten Organe im
menschlichen Körper. Die Gründe für die Besonderheit dieses Organs sind aber vor allem in der
Evolution der Pankreatologie, den Teilbereich der Medizin, der sich der Erforschung der
Bauchspeicheldrüse widmet, zu finden.
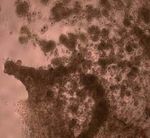
Seine kaum zugängliche Lage in der Tiefe des Bauchhöhle,
an der Kreuzungstelle mehrerer lebenswichtiger Gefäße, Nerven und
seines “monotones”, einfarbiges Aussehen (Abb. 1) haben dazu
geführt, dass es lange Zeit in der Antike im Gegensatz zu den
übrigen wichtigen Bauchorganen unerkannt blieb. Herophilus von
Chalcedon (Abb. 2), der ca. 300 v. Chr. dieses Organ erstmalig
beschrieb, konnte mit diesem “wie Fleisch aussehenden” Organ nicht
viel anfangen und gilt heute noch als der Namensgeber pan-kreas,
griechisch “alles Fleisch”. Die antiken Nachfolger von Herophilus, Abb. 1: Lage des Pankreas
darunter auch Aristoteles und Galen, konnten zum
Verständnis der Funktion des Pankreas nichts beitragen und wiesen ihm
lediglich eine Rolle als mechanische Stütze für den Magen und das Omentum,
dem Bauchnetz, zu. Erst 1600 Jahre nach Galens Tod, erkannte der
französische Physiologe Claude Bernard die essentielle Rolle des Pankreas in
der Verdauung von Fetten und Proteinen. Diese neuen Erkenntnisse
ermöglichten erstmals die Verknüpfungen von Störungen innerhalb des
Pankreas, das für die damals noch unerklärlichen Verdauungsprobleme des
Abb. 2: Herophilus
Menschen mitverantwortlich zu sein schien. Spannenderweise erwiesen sich
die Störungen dieses Organs, dessen Mysterium nur teilweise erst zum 2000. Geburtstag der
Naturwissenschaften entschlüsselt werden konnte, als Hauptdarsteller in der Volkskrankheit
Diabetes. Dies war erst möglich nachdem 1922 Drs. Banting und Best die Isolation des
Hauptbotenstoffes der Zuckerverwertung, das Insulin, aus dem Pankreas gelungen war.
Die nachfolgenden medizinischen Fortschritte im 20. Jahrhundert haben nicht nur eine
Verlängerung der menschlichen Lebenswartung ermöglicht, sondern auch wegen des
demographischen Wandels den Fokus der Pankreatologie auf die tückischste und bösartigste
Pankreaserkrankung, den Bauchspeicheldrüsenkrebs bzw. das Pankreaskarzinom, gerichtet. Die
Bezeichnung “tückisch” verdient diese Krebsart vor allem deswegen,
weil sie lange Zeit keine Beschwerden bei den Betroffenen verursacht
und dadurch meistens erst in fortgeschrittenen Stadien mit Schmerzen
entdeckt wird, in denen sie auch kaum mehr therapierbar ist. Wie bei
fast allen Krebsarten besteht die einzige Möglichkeit zur Heilung der
Patienten in der chirurgischen Entfernung des Geschwulstes aus dem
Pankreas. Leider erwies sich seit dem Anfang des 20 Jahrhunderts bis
1950’er auch die chirurgische Entfernung der bösartigen
Pankreasgeschwülste als ein Mysterium: Der Wiederanschluss des
Restpankreas an den Darm nach Entfernung des Tumors war technisch
außerordentlich schwierig, und die meisten Patienten, die bis Mitte des Abb. 3: Dr. Allen O. Whipple
20 Jh. operiert wurden, verstarben an den chirurgischen Komplikationen. Der amerikanische
Chirurg Allen O. Whipple (Abb. 3), nach dem die heute noch gültige Operation zur Enfernung
des Pankreastumors benannt ist, vermerkte 1935, dass die Pankreaschirurgie selbst von den
1begabtesten Chirurgen seiner Zeit als “unzulässig” wahrgenommen wurde. Erst nach Einführung
neuer, resistenterer chirurgischer Nahtmaterialien, von Bluttransfusionen, nach Entdeckung des
gerinnungsfördernden “Vitamin K” und durch erneute Versuche von chirurgischen Pionieren wie
Whipple gelang es, die Komplikationsrate von Pankreasoperationen in großen chirurgischen
Zentren auf seine heutigen Werte von unter 5 % zu reduzieren.
Die Chirurgen des 21. Jahrhunderts beschäftigen sich heut zu Tage nicht nur mit der
Optimierung ihrer chirurgischen Techniken, sondern auch gleichzeitig mit der Erforschung der
Entstehungsmechanismen des Pankreaskarzinoms. Diese Erkrankung, von der alleine in
Deutschland jährlich ca. 13.000 Menschen betroffen sind, ist häufig mit quälenden und nicht
ertragbaren Bauchschmerzen assoziiert, die die
Betroffenen während ihrer limitierten Lebenszeit
begleiten. Die Arbeitsgruppe “Neuropathie und
Schmerz bei Pankreaserkrankungen” unter der
Leitung von Dr. Güralp O. Ceyhan am Klinikum
Rechts der Isar beschäftigt sich genau mit diesem
wichtigen Aspekt und hat sich der Erforschung der
Entstehung des Pankreasschmerzes und der
möglichen Rolle des Nervensystems im
Pankreaskarzinom gewidmet. Seit Anfang der 90’er Abb. 4: Links: Ein normaler, unauffälliger Nerv aus
dem Pankreas. Rechts: Ein Nerv (braun gefärbt) im
Jahre wissen wir, dass die Krebszellen im Rahmen Pankreas, in dem Krebszellen (violette Bezirke, siehe
der Entstehung des Pankreaskarzinoms sehr häufig Pfeile) zu sehen sind.
und gezielt die Nerven im und sogar auch
unmittelbar außerhalb des Pankreas befallen. Dabei beschränken sie sich nicht auf einen Befall
des Gewebes um die Nerven, sondern dringen oft durch die äußere Schutzhülle (Perineurium) der
Nerven ins Innere der Nerven (Endoneurium) ein und zerstören dabei die Nervenarchitektur.
Somit sind die freiliegenden
Nervenfasern schutzlos diversen
Giftstoffen, Entzündungsvermittlern
und Krebszellen unmittelbar
ausgesetzt. Hierbei nutzen die
Karzinomzellen die Nervenhülle der
Nerven wie einen
„Autobahntunnel“, in dem sie sich
Abb. 5: Links: Normales Pankreas: keine Nerven sichtbar, rechts: Pankreas- ungehindert fortbewegen, wachsen
karzinomgewebe, in dem die vergrößerten Nerven mit Pfeilen markiert sind. und in andere Organe streuen
können. Durch diese zielgerichtete
Bewegung der Krebszellen in und entlang der Nervenhülle ist es für den Chirurgen meist sehr
schwierig eine kurative (heilende) Entfernung des Pankreastumors zu erreichen. In diesem
Zusammenhang konnte die Arbeitsgruppe von Dr. Ceyhan ganz neue Perspektiven im Bereich
der “pankreatischen Neurobiologie” eröffnen: Sie konnten erstmals zeigen, dass es innerhalb des
Pankreaskarzinoms zu einer Hypertrophie/Vergrößerung und Dichtezunahme dieser Nerven
kommt (Abb. 5) und dass das Pankreaskarzinom Wachstumsfaktoren ausschüttet, die das weitere
Wachstum und Aussprossung der Nerven günstig beeinflusst.1-3 Die Folge dieser
Mehranreicherung und Hypertrophie von pankreatischen Nerven war die proportionale
Steigerung der Invasion der pankreatischen Nerven mit Krebszellen und Entzündungszellen.1
Hierbei war der Schweregrad der nervale Befall von Krebszellen umso ausgeprägter, umso
2prominenter die pankreatischen Nervenveränderungen waren.1 Entscheidend für die Bedeutung
dieser Entdeckung ist, dass diese Veränderungen nicht nur auf mikroskopischer Ebene
feststellbar sind, sondern dass diese auch einen direkten Einfluss auf das allgemeine
Wohlempfinden und das Überleben der Patienten haben. Patienten mit ausgeprägten
Veränderungen der pankreatischen Nerven mit Größen- und Dichtezunahme sowie
hervorstechendem Befall mit Krebszellen, litten deutlich länger und öfter an schweren und mit
Schmerzmitteln schwer zu kontrollierbaren Bauchschmerzen.1 Darüberhinaus war der
Schweregrad des Pankreas-Schmerzes unmittelbar mit dem Überleben der Patienten assoziiert.
Im Klartext, Patienten mit ausgeprägten Nervenveränderungen und Schmerzen lebten deutlich
kürzer, als die Patienten die wenig oder keine Nervenveränderungen und Schmerzen aufwiesen.1
Aus diesen neuen Erkenntnissen resultierte die international anerkannte Bezeichnung der
Schmerzen, an denen die Pankreaskarzinompatienten leiden, als “neuropathisch”, also als ein
Schmerz, der unmittelbar durch unterschiedliche Schäden an einem Nerven bedingt ist.1, 4 Dieses
neue Bewusstsein eröffnet ganz neue Therapiemöglichkeiten und –Ansätze, denn Schmerzen
vom neuropathischen Typ werden nach neuesten wissenschaftlichen Erkenntnissen ganz anders
behandelt, als die vom üblichen, “nozizeptiven” Typ. Hiermit konnten diese Entdeckungen der
Arbeitsgruppe Dr. Ceyhan einen neuen “Paradigmenwechsel” in der Pankreatologie bewirken.
Abb. 6: Links und Mitte: die Anordnung der Krebs- und Nervenzellen zueinander. Rechts oben: Krebszellen, die auf der den
Nervenzellen zugewandten Seite liegen, bilden Gruppen und starten die Invasion. Rechts unten: Die Krebszellen, die der zellfreien
Seite zugewandt sind, zeigen dahingegen keine Reaktion.
Nun stellte sich die Frage, warum die Krebszellen ausgerechnet von den Nerven so stark
angezogen werden und diese als einen primären Metastasierungsweg aussuchen? Um dies zu
beantworten, entwickelte die Arbeitsgruppe von Dr. Ceyhan ein neuartiges 3D-Modell, das Ihnen
ermöglichte, die unmittelbaren Interaktionen der Nerven mit den Krebszellen in einem
künstlichen Umfeld zu simulieren und zu studieren.5 Hier zeigten Sie in einer beeindruckenden
Weise, dass die Krebszellen im indirekten Kontakt mit den Nervenzellen sich deutlich in ihrer
3Gestalt und ihrem Verhalten änderten und zielstrebig die isolierten Nervenzellen befielen. Sie
bildeten Krebszell-Gruppen um die Nerven herum und zeigten dabei Krebszellausläufer, die
direkt auf die Nervenfasern ausgerichtet waren. Die Ergebnisse erweckten den Eindruck, als ob
die Nerven mit den Krebszellen kommunizierten, lange bevor sie überhaupt in einen direkten
Kontakt miteinander standen. Mit diesem Modell war es nun möglich das Phänomen der nervalen
Invasion von Krebszellen nachzuahmen und erste Veränderungen, die mögliche Erklärungen zur
Entstehung dieses Phänomens bieten, zu entdecken.5 Weiterhin konnten Dr. Ceyhan und seine
Mitarbeiter auch mehrere molekulare Botenstoffe identifizieren, die von den Krebszellen in
diesem Prozess gebildet und ausgeschüttet werden. In der Zukunft erwarten wir, mit der
Erkenntnis dieser Voruntersuchungen, mögliche therapeutische Ansätze zu definieren und in der
Klinik einzusetzen.
Unter Anwendung ihres neuen und mittlerweile wissenschaftlich anerkannten 3D-
Modells5 zur Untersuchung der Entstehungsmechanismen der nervalen Invasion von Krebszellen
möchte die Arbeitsgruppe von Dr. Ceyhan auf ihren bisherigen Vorarbeiten aufbauen. Hierbei
möchten Sie sich unter Nutzung ihres Modells auf folgende Punkte konzentrieren:
1. Nachweis von potentiellen Schlüsselfaktoren die die Aggressivität der Pankreas-
Krebszellen steigern und somit zu einer ausgeprägten nervalen Invasion führen.
2. Bestimmung von entscheidenden Botenstoffen, die von den Nerven ausgeschüttet werden
und die Krebszellen in ihrem Wachstums- und Fortbewegungsverhalten positiv
unterstützen.
Mit den Ergebnissen aus Punkt 1. + 2. ist es möglich molekulare Botenstoffe mit
molekularbiologischen Techniken in den beteiligten Zellen gezielt auszuschalten. Hiermit können
deren Einfluss innerhalb der Nerven-Krebs-Interaktionen charakterisiert werden und weiter
untersucht werden, ob diese eine mögliche therapeutische Plattform bieten, die das Fortschreiten
der nervalen Invasion in Pankreaskarzinom-Patienten verhindern kann.
3. Weiterhin gilt es herauszufinden, welchen Einfluss das umgebende Gewebe auf die
Krebszellen und Nerven in diesem Zusammenhang hat. Wir wissen aus eigenen
Vorarbeiten, dass die Invasion der Nerven durch Krebszellen vor allem in
bindegewebsreichen Teilen des Pankreas stattfindet.1 Die sogenannten Sternzellen des
Pankreas sind die Hauptproduzenten des Bindegewebes im Pankreas. Daher wird die
Erforschung der potentiellen Einflüsse der Sternzellen auf die Entstehung der nervalen
Invasion eine entscheidende Rolle spielen. Hierzu wird das neu etablierte 3D-Modell die
Wechselwirkung zwischen Krebszellen, Sternzellen und Nervenzellen näher untersuchen
und charakterisieren.
Abschließend läßt sich zusammenfassen, dass die gezielte Beeinflussung der
Wechselwirkung zwischen den Krebszellen und dem Nervensystem im Pankreaskarzinom eine
bisher wenig erforschte, aber aufgrund der neusten Ergebnisse eine viel versprechende
Therapieoption beim Bauchspeicheldrüsenkrebs darstellt. Der Bauchspeicheldrüsenkrebs ist die
vierthäufigste Krebstodesursache in der zivilisierten Welt. Auch heute noch leben im
Durchschnitt lediglich 5 aus 100 Patienten mit dieser tückischen Erkrankung länger als 5 Jahre
nach der Feststellung der Diagnose. Das Kapitel “Pankreas” in dem weltweit bekanntesten
amerikanischen Chirurgie-Lehrbuch “Schwartz’s Principles of Surgery” beginnt mit dem Satz
“Das Pankreas ist das gnadenloseste Organ im menschlichen Körper, das die meisten Chirurgen,
wenn nicht unbedingt notwendig, meiden anzufassen ”. Daher ist uns ein großes Anliegen, dass
4im Sinne des Patienten die chirurgische Forschung von heute, den Chirurgen von morgen mit
dem von uns noch zu ermittelnden Daten, hoffentlich das Verständnis und den Umgang mit der
Bauchspeicheldrüse erleichtern soll.
Literatur:
1. Ceyhan GO, Bergmann F, Kadihasanoglu M, Altintas B, Demir IE, Hinz U, Muller MW,
Giese T, Buchler MW, Giese NA, Friess H. Pancreatic neuropathy and neuropathic pain--a
comprehensive pathomorphological study of 546 cases. Gastroenterology 2009;136:177-
186.
2. Ceyhan GO, Bergmann F, Kadihasanoglu M, Erkan M, Park W, Hinz U, Giese T, Muller
MW, Buchler MW, Giese NA, Friess H. The neurotrophic factor artemin influences the
extent of neural damage and growth in chronic pancreatitis. Gut 2007;56:534-544.
3. Ceyhan GO, Giese NA, Erkan M, Kerscher AG, Wente MN, Giese T, Buchler MW, Friess
H. The neurotrophic factor artemin promotes pancreatic cancer invasion. Ann Surg
2006;244:274-281.
4. Ceyhan GO, Michalski CW, Demir IE, Muller MW, Friess H. Pancreatic pain. Best Pract
Res Clin Gastroenterol 2008;22:31-44.
5. Ceyhan GO, Demir IE, Altintas B, Rauch U, Thiel G, Muller MW, Giese NA, Friess H,
Schafer KH. Neural invasion in pancreatic cancer: a mutual tropism between neurons and
cancer cells. Biochem Biophys Res Commun 2008;374:442-447.
5Sie können auch lesen