Nahrungsmittel-Allergien-Nahrungsmittel-Intoleranzen - Labors.at
←
→
Transkription von Seiteninhalten
Wenn Ihr Browser die Seite nicht korrekt rendert, bitte, lesen Sie den Inhalt der Seite unten
LABORS.AT
ThermoFischer Scientific
Mittwoch, 18. April 2018
Wien
Nahrungsmittel-Allergien-
Nahrungsmittel-Intoleranzen
Lili Kazemi-Shirazi
Klinik für Innere Medizin III
Abt. für Gastroenterologie & Hepatologie
Medizinische Universität Wien
Klinische Abteilung für
Gastroenterologie und Hepatologie
Univ.Klinik für Innere Medizin III
1Allergie Intoleranz
Erworbene Überempfindlichkeit
Überreaktion des ohne Beteiligung des
Immunsystems; Immunsystems
Toleranz möglich
Beispiel Milchunverträglichkeit
Kuhmilchallergie: Laktoseintoleranz:
→Sojamilch →Laktosefreie ProdukteSubakut-
chronisch
v.a. Haut, GI
IgE vs non-IgE mediierte vs gemischte NM-Allergien
Cave Anaphylaxie!UpToDate®
Turnball JL et al, APT 2015
IgE-mediierte NM-Allergie
• 6-8% der Kinder
– Kuhmilch, Ei, Soja, Erdnuss, Nüsse, Fisch,
Schalentiere, Weizen
• 3-4% der Erwachsenen
– Primär: selten
• Erdnuss, Nüsse, Fische, Schalentiere
– Sekundär: häufig, Kreuzallergie mit Pollen
• Orales Allergie Syndrom (OAS)
• Birke: Äpfel, Nüsse
• Beifuß: Sellerie, Karotte, Gewürze 5Orales Allergie Syndrom (OAS)
Pollen-food allergy syndrome (PFAS)
Mechanismus: Kreuzallergie (homologe Proteine/Epitope)
JACI 2017
Kazemi-Shirazi et al, Int Arch Allergy Immunol 2002
Kazemi-Shirazi L et al, JACI 2000 6NM-Allergie: Symptome
• Nach Zufuhr von Nahrungsmitteln
• Symptome
– Übelkeit, Erbrechen, Bauchschmerz, Durchfall
– Flush, Pruritus, Urtikaria, Angiödem
– Giemen
– Benommenheit,Synkope
UpToDate®
Turnball JL et al, APT 2015 8Anaphylaxie: Definition und Ursachen
• schwere, lebensbedrohliche, generalisierte od.
systemische Überempfindlichkeitsreaktion
• Am häufigsten:
– Wespen-, Bienenstich
– Medikamente
– Nahrungsmittel
• Sonderform (selten):
Food dependent exercise-induced anaphylaxis
• Tryptase Erhöhung
UpToDate®
Turnball JL et al, APT 2015Einteilung der Grade der Anaphylaxie nach Ring und Mesmer
(Schleim)Haut GI-Trakt Atemwege Herz/Kreislauf
Juckreiz, Urtikaria
I Flush, Angioödem
- - -
Rhinitis Tachykardie
Juckreiz, Urtikaria Nausea Anstieg ≥ 20/min
II Flush, Angioödem Krämpfe
Heiserkeit
Blutdruckabfall ≥ 20
Laryng. Dyspnoe mm Hg
Larynxödem
Juckreiz, Urtikaria Erbrechen Schock
III Flush, Angioödem Defäkation
Bronchospasmus
Bewusstlosigkeit
Zyanose
Juckreiz, Urtikaria Erbrechen Atemstillstand oder
IV Flush, Angioödem Defäkation Herz-/Kreislaufstillstand
Ring et al; Allergo J 2007; 16: 420–34Beteiligung verschiedener Organsysteme bei anaphylaktischen Reaktionen
(2012 Patienten aus Deutschland, Österreich, Schweiz)
2500
gesamt
2000
Haut
84%
Herz-Kreislauf
72% Atmung
1500 68%
1000 GI-Trakt
40%
500
0
Worm M, Allergy 2012Diagnostik bei NM-Allergie
• Anamnese
– Das Wichtigste!
• Hauttest
– Pricktest mit kommerziellen Extrakten
– Prick-by-prick mit frischen NM
• In vitro Tests (Ergebnis in kUA/L) Auswahl und
– Immunoassays (RAST, FEIA) Interpretation
– Messung Gesamt-IgE im Serum in Kontext zu Klinik!
– Nachweis NM-spezifischer IgE im Serum
– Komponenten-spezifische Tests
• zB:Erdnuss: Ara h 2 (stabil, schwere Reaktion), Ara h 8 (labil)
• Ernährungsprotokoll
• Eliminationsdiät
– Entfernen einzelner NM, „oligoantigen“, Elementardiät
• Provokation (Spezialfragestellung; cave Anaphylaxie! )
UpToDate®
Turnball JL et al, APT 2015Diagnose IgE-mediierter NM-Allergien
Konzentration
Reaktion von Mastzellen der zirkulierender IgE
Haut gegenüber Allergen
Reaktion
zirkulierender
Basophiler
gegenüber
Allergen
Santos AF et al, JACI 2017UpToDate®; Turnball JL et al, APT 2015
Hauttest oder in vitro Test?
Haut Test In vitro Test
• Meist sensitiver • Breit verfügbar
• Billiger • Durch Antihistaminika nicht
• Ergebnis sofort verfügbar beeinflusst
• Nützlich bei Pat. mit schwerer
Anaphylaxie
(Risiko durch Hauttest!)
• Schwere atopische
Dermatitis, Dermographismus
Positiver Haut-od. in vitro Test alleine ≠ Allergie,
sondern Sensibilisierung, daher ANAMNESE!Griffiths RLM et al, Int Arch Allergy Immunol 2017 Bester Test: SPT: Latexallergie ImmunoCAP: Nuss-, Weizenallergie, Spezifische NM Anaphylaxie ISAC: OAS
IgG oder IgG4 basierten Tests
• Nicht validiert
• Typisch: multiple positive Ergebnisse
• Kann normale Immunantwort gegenüber
NM repräsentieren
• Hinweis auf Toleranz
Beyer K, Teuber SS, Curr Opin Allergy Clin Immunol. 2005
Aalberse RC et al, Clin Exp Allergy. 2009
Hochwallner H et al, Allergy 2011NM-Allergie: Therapie
• Allergenvermeidung
– Oft theoretisch einfacher als in der Praxis
– Etikettierung beachten
• Epipen® und Schulung (Anaphylaxie!)
• Primäre Prävention von NM-Allergien
– Einführen von Erdnüssen zw. 4-6 LM
– Eier bei (Hochrisiko) Säuglingen zw. 4-6 LM ?
• Allergen-Immuntherapie (AIT)
– orale -(OIT)/sublinguale-/epikutane IT UpToDate®
Turnball JL et al, APT 2015
– Derzeit Studien, nicht Routine Wei-Liang Tan J, JACI 2017
Bellach J, JACI 2017
Palmer DJ, JACI 2017
• Biologika Natsume O, Lancet 2017
Du Toit G, JACI 2008
– Omalizumab? Vickery BP et al, JACI 2017
MacGinittie AJ et al, JACI 2017
Sampson HA, JAMA 2017Beeinflussung des Mikrobioms: neue Therapie Methode für NM-Allergien? Gesund Plunkett CH et al, JI 2017 Dysbiose
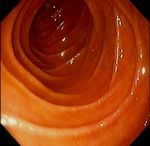
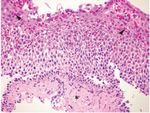
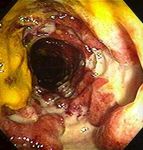
Eosinophile Ösophagitis (EoE) • Chronische, immun-mediierte ösophageale Erkrankung • ösophageale Symptome und eosinophile Entzündung - Leitsymptome : Dysphagie, NM-Bolus, Brustschmerz • Ausschluss anderer Ursachen für ösophageale Eosinophilie Mindestens 6 Biopsien ! Kia and Hirano, Nat Rev Gastroenterol Hepatol 2015 Histo für Diagnose und Monitoring! Lucendo AJ, UEJ Journal 2017
Eosinophile Ösophagitis (EoE)
Kia and Hirano , Nat Rev Gastroenterol Hepatol 2015GERD oder PPI-REE oder EoE?
Molina-Infante J, Gut 2016Jorveza® „empiric
(Budesonid Schmelztablette) 6 food ED“
Lucendo AJ, UEJ Journal 2017„Gluten (Weizen) -
Unverträglichkeit“
Zöliakie Weizen- WIS
(immun-mediiert) Allergie (NCWS)
Dermatitis (IgE-mediiert) (NCGS)
Herpetiformis
(immun-mediiert)Zöliakie: Chamäleon der Inneren Medizin
• Prävalenz:
• Europäer: 1:100-1:500 je nach Studien, also etwa 1%
• Auftreten aber auch in Nordafrika, Naher Osten ,
Indien, China
• Kindesalter: 50%
– auch bis 80 L.J.
24Pathogenese
• Eine Autoimmunerkrankung
– Autoantigen: Tissue Transglutaminase (TG2), ein
Enzym im Endomysium
• Bei genetisch prädisponierten Individuen
– HLA (DQ2 und DQ8 )- und non-HLA Gene
• Trigger: Umweltfaktoren
– Gluten (Proteingemisch in Samen von Getreide)
• Weizen, Gerste, Roggen, Hafer
– Stillen, Infekte, MedikamenteDiagnose der Zöliakie
• Klinische Symptome
• Zöliakie assoziierte Antikörper (Serologie)
• HLA DQ2/DQ8 (Genetik)
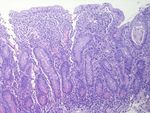
• Histologie (Duodenalbiopsien)
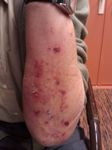
Husby S, Murray AJ, Mayo Clin Proc 2013 26Klinische Manifestationen 27
Bildquelle:
Wikipedia
• Blähungen
• Stuhlveränderungen
• Gewichtsverlust
• Bauchschmerzen
• Eisenmangelanämie
• Osteopenie (↓ Vitamin D und Calcium; ↑ AP)
• Neuropsychiatrisch (↓ B Vitamine)
– Kopfschmerzen, Depression, periphere
Neuropathie, Ataxie, Epilepsie, Angststörung
• Extremform: Zöliakie Krise!
• Bis 60% keine typische Symptomatik!
– Müdigkeit, Erhöhte Transaminasen, Eisenmangel
– asymtomatischZöliakie: Subklinische Erkrankung Diagnose wichtig aus folgenden Gründen: • Zöliakie assoziierte Komplikationen • Nährstoffdefizite • Auftreten von mit Zöliakie assoziierten Autoimmunerkrankungen – v.a. gemeinsame genetische Prädisposition • Screening von Familienangehörigen
Bildquelle: „UpToDate“ Antikörper Sensitivität Spezifizität
29
IgA EMA 85-98% 97-100%
Zöliakie Serologie
IgA tTG 90-98% 95-97%
IgA DGP 94% 99%
IgG DGP 92% 100%
– IgA endomysiale Ak (IgA EMA): Immunfluoreszenz
höchste
höchste
diagnostische
– IgA tissue transglutaminase Ak (IgA tTG): ELISA diagnostische
Genauigkeit
Genauigkeit
– Gesamt IgA ↓ >>> IgG EMA, IgG TTG
– Anti-Gliadin-Ak (IgA AGA, IgG AGA): „out“ für Routine
• Häufig falsch positiv (15-20%!)
– Ak gegen Deamidiertes Gliadin Peptid (IgA DGP, IgG DGP)
• 2. Generation AGA TestHLA-DQ2 und HLA-DQ8
• Fast alle Patienten mit Zöliakie DQ2/DQ8+
– DQ2+: 95%; DQ8+: Rest
• Aber auch 30-35% der Bevölkerung
– Nur 2-5% davon entwickeln Zöliakie
– HLA Haplotypen notwendig, aber nicht
ausreichend, um Zöliakie zu entwickeln
• Wertigkeit von DQ2 und DQ8: wenn negativ,
Zöliakie ausgeschlossen
– Hoher negative predictive value31
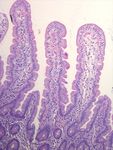
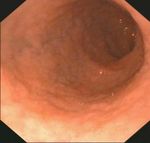
Gesundes Duodenum
Duodenum bei
Zottenatrophie
Marsh 3c32
Management:Gluten freie Diät (GFD)
• Strikte lebenslange glutenfreie Diät
– verboten:
• Weizen-, Roggen-, Gerste-, Dinkel-,Grünkern-, Kamutprodukte
– erlaubt:
KEINE Gluten-freie
• Reis-, Mais-, Diät
Kartoffelmehl, Quinoa, (GFD) VOR
Amarant
– Eher erlaubt (rein)
serologischer
• Hafer und endoskopischer
– Probleme:
Diagnosesicherung!
• Backpulver, Bier, Fertigprodukte, Abschmecken von glutenhältigen
Soßen,Gasthausessen, Bäcker (die keine Spezialbäcker)
– Empfehlenswert:
• Beratung durch Diätassistentin, Mitgliedschaft bei ARGE ZöliakieWheat Intolerance Syndrome (WIS)
33
(Non-Celiac wheat sensitivity; NCWS)
(Non-Celiac gluten sensitivity; NCGS)
• Eine Ausschlussdiagnose
– Zöliakie ausgeschlossen
• Serologie neg., Duodenal-Bx normal
– Weizenallergie ausgeschlossen
• neg. IgE und Hautpricktest
• Beschwerden bessern sich unter Weizenentzug (GFD) und treten nach
Wiedereinführen von Weizen (nicht aber unbedingt Gluten!) wieder auf
• Prävalenz 0.6-13% der Bevölkerung
• Überlappung mit RDS?
• Mögliche Rolle von Amylase-Trypsin Inhibitoren (ATIs)
– Sind Getreideproteine
• Rolle von FODMAPs
• Therapie:
Ellis A, et al, Lancet 1978
– Elimination aller Weizen-enthaltenden Produkte Junker Y, et al, J Exp Med 2012
– Evtl. FODMAP reduzierter Diät Biesiekierski JR, et al Gastro 2013
Jericho H et al, JPGN 2017
Molina-Infante J, Clin Gastroenterol Hepatol 2017FODMAP reduzierte Diät bessert RDS Symptome
• Fermentable Oligo-, Di-, Monosaccharides And Polyols
• FODMAPS umfassen:
– Fruktane (zB in Gemüse, Getreide), Galaktane (zB
Hülsenfrüchte), Laktose, Fruktose, Polyole (zB Sorbit, Xylit)
• Reduktion von schlecht absorbierbaren Kohlenhydrate
Gibson & Shepherd , Am J Gastroenterol 2012
Halmos EP, Gastro 2014 34Functional Bowel Disorders (FBD)
Lacy BE, Gastro 2016Chron. Entz. Darmerkrankung (CED) oder RDS?
CED: von Entzündung bis zur irreversiblen Schädigung
ZEIT IST DARM!!
Point of no return!
Colitis ulcerosa
Ziel: Mukosale Heilung
Pariente et al, IBD 2011
M. CrohnRDS vs CED: Fäkales Calprotectin (FC) Calcium-bindendes Protein neutrophiler Granulozyten • Anstieg: Granulozyten gelangen durch Darmwand ins Darmlumen (gestörte Barriere) • ELISA • Normalwert:
38
Laktoseintoleranz
• Häufig
– Prävalenz: 7-20% Kaukasier; 65-75% Afrikaner; bis 90% in Ostasien
• Laktase (Enzym) im Dünndarm
– Spaltet Laktose (Disaccharid) in Glukose+Galaktose
(Monosaccharide>werden absorbiert)
• Laktasemangel
– Laktose wird nicht in Dünndarm absorbiert>gelangt in
Dickdarm>Substrat für Bakterien>Beschwerden
• Symptome:
– abdominell Krämpfe, Blähungen, Flatulenz, Diarrhoe
– DD: Reizdarm!Ursachen der Laktoseintoleranz
• Primäre Laktosemalabsorption
– Ethnisch (LCT-Gen)
• häufigste Ursache, genetisch regulierte ↓ Laktase Aktivität
• „Lactase non-persistence“: Asien, Afrika
• „Lactase persistence“: Kaukasier
– Hereditärer Laktasemangel
• Sehr selten, autosomal-rezessiv, fehlende Laktase Aktivität
– Frühgeborene
• Sekundäre Laktosemalabsorption
– Dünndarmerkrankungen:
• Zöliakie, Lambliasis, akute Gastroenteritis, M.Crohn-Jejunum,
Bacterial overgrowth
– Schnelle Passage:
• Magen-, Dünndarmresektionen , KurzdarmsyndromDiagnostik der Laktoseintoleranz • Laktosetoleranz Test (Blut) – 50g Laktose oral>BZ nach 0, 60 und 120 Min messen – Positiver Test: Anstieg des BZvorher und danach Atem H2 messen – Positiver Test: Atem-Wasserstoff Anstieg >20 ppm • Gentest: Laktase Gen (LCT) – T>C Polymorphismus legt Menge an gebildeter Laktase fest – LCT-Genotypen: CC, TC, TT – CC: genetische Anlage für Laktoseintoleranz – T-Allel: Laktase-Persistenz
• Exzellente Korrelation zwischen
CC Genotyp und positivem H2 Test
(97% hatten auch positiven L-H2-Test)
• Korrelation weniger stark zwischen
TC oder TT Genotyp und negativem H2 Test
(86% hatten negativen L-H2-Test)
Eur J Gastro Hepatol 2005
41Therapie der Laktoseintoleranz Diät : Reduktion/Meiden von Produkten, die Laktose enthalten: – Milch und Milchprodukte • Milcheis, Vollmilchschokolade, Käse, ... – Industrielle Produkte • Fertigpuddings, Soßen, ... Laktasepräparate: Aber nur 50% Verdauung Einnahme zu den Mahlzeiten
Fruktoseintoleranz • Häufigkeit – Bis zu 50% bei Dyspepsie • Ursache – Defekt des GLUT-5-Transporters (Jejunalzelle) – Angeboren oder Erworben • Diagnose – Fruktose-H2-Test (25 g Fruktose) – Positiver Test: Atem-Wasserstoff Anstieg >20 ppm • Cave: Hereditäre Fruktoseintoleranz (Fruktosämie)! – Hypoglykämie nach Fruktosekonsum
Therapie der Fruktoseintoleranz
• 2 Formen von Fruktose
– Monosaccharid und Disaccharid
(Saccharose=Glucose-Fruktose)
– Absorption als Disaccharid > Monosaccharid
• Wichtig:
– Fruktose-Gehalt
– Welche anderen Zucker werden miteingenommen?
• Glukose erleichtert , Sorbit erschwert Fruktose Aufnahme
• Vermeiden von Nahrungsmittel mit hohem
Nettogehalt an FruktoseTherapie der Fruktoseintoleranz • Säfte und Früchte mit hohem netto Fruktosegehalt – Äpfel, Birnen, Kirschen, Pflaumen, Datteln • Getränke mit Fruktose Maissirup • Honig • Sorbithältige Kaugummis und Süßigkeiten (Cave „Zuckerfrei“!)
Histamin-Intoleranz
Mangel an
Diamine Oxidase
Mainz and Novak, Am J Clin Nutr 2007Histamin medierte Symptome
Mainz and Novak, Am J Clin Nutr 2007Take home Messages • NM-Allergie: selten, Immunsystem beteiligt – Anamnese das Wichtigste! – In vitro Diagnostik und Hauttest hilfreich – Anaphylaxie: Tryptase • NM-Intoleranz: häufig, Enzymmangel, Transporterdefekt – H2 Tests, LCT-Gen • An EoE denken! • Zöliakie Screening: EMA und TTG (DGP) • Funktionelle vs organische Darmerkrankung: Calprotectin
DANKE FÜR IHRE AUFMERKSAMKEIT!
lili.kazemi-shirazi@meduniwien.ac.at
49Sie können auch lesen