www.kup.at/speculum Online-Datenbank mit Autoren- und Stichwortsuche - Krause und Pachernegg
←
→
Transkription von Seiteninhalten
Wenn Ihr Browser die Seite nicht korrekt rendert, bitte, lesen Sie den Inhalt der Seite unten
Geburtshilfe ∕ Frauen-Heilkunde ∕ Strahlen-Heilkunde ∕ Forschung ∕ Konsequenzen
Leitlinie für die Diagnose und Therapie von
Cervikalen Intraepithelialen Neoplasien (CIN) und
Mikrokarzinomen der Cervix uteri
Speculum - Zeitschrift für Gynäkologie und Geburtshilfe 2005; 23 (3)
(Ausgabe für Schweiz), 20-20
Speculum - Zeitschrift für Gynäkologie und Geburtshilfe 2005; 23 (3)
(Ausgabe für Österreich), 20-25
Homepage:
www.kup.at/speculum
Online-Datenbank
mit Autoren-
und Stichwortsuche
Krause & Pachernegg GmbH • Verlag für Medizin und Wirtschaft • A-3003 Gablitz
P.b.b. 02Z031112 M, Verlagsort: 3003 Gablitz, Linzerstraße 177A/21e-Abo kostenlos
Datenschutz: Das e-Journal
Ihre Daten unterliegen dem Datenschutzgesetz und Speculum
werden nicht an Dritte weitergegeben. Die Daten
werden vom Verlag ausschließlich für den Versand ✔ steht als PDF-Datei (ca. 5–10 MB)
der PDF-Files des Journals Speculum und eventueller stets internetunabhängig zur Verfügung
weiterer Informationen das Journal betreffend ge-
nutzt. ✔ kann bei geringem Platzaufwand
gespeichert werden
Lieferung:
Die Lieferung umfasst die jeweils aktuelle Ausgabe ✔ ist jederzeit abrufbar
des Journals Speculum. Sie werden per E-Mail ✔ bietet einen direkten, ortsunabhängigen
informiert, durch Klick auf den gesendeten Link er
Zugriff
halten Sie die k omplette Ausgabe als PDF (Umfang
ca. 5–10 MB). Außerhalb dieses Angebots ist keine ✔ ist funktionsfähig auf Tablets, iPads
Lieferung möglich. und den meisten marktüblichen e-Book-
Abbestellen: Readern
Das Gratis-Online-Abonnement kann jederzeit per ✔ ist leicht im Volltext durchsuchbar
Mausklick wieder abbestellt werden. In jeder Benach-
richtigung finden Sie die Information, wie das Abo ✔ umfasst neben Texten und Bildern
abbestellt werden kann. ggf. auch eingebettete Videosequenzen.
www.kup.at/speculum23. Jahrgang, 3/2005
Die verwendete histologische Terminolo-
gie entspricht der histologischen Klassifi-
kation der WHO (Tabelle 1). Die kolposko-
Leitlinie für die Diagnose und pische Terminologie entspricht der No-
menklatur der International Federation of
Therapie von Cervikalen Intra- Cervical Pathology and Colposcopy (IFCPC),
Barcelona 2002, in der deutschsprachigen
epithelialen Neoplasien (CIN) und Version (Tabelle 2). Die Ergebnisse der Zy-
tologie werden entsprechend der Leitlinien
Mikrokarzinomen der Cervix uteri der Österreichischen Gesellschaft für Zyto-
logie zur Nomenklatur und zervixzytolo-
gischen Befundwiedergabe (Version 2005)
wiedergegeben (Tabelle 3).
Erstellt von der
AGK (Arbeitsgemeinschaft für Kolposkopie in der
ÖGGG): G. Breitenecker1, F. Girardi2, E. A. Joura3, Tabelle 1: Histologische Klassifikationen der zervikalen Läsionen
P. Kohlberger3, O. Reich4, A. Widschwendter5
Dysplasie leicht mäßig schwer/
(in alphabetischer Reihenfolge) Carcinoma in situ (Cis)
geringgradig mittelggradig hochgradig
und der CIN, Grad I II III
AGO (Arbeitsgemeinschaft für Gynäkologische SIL LG-SIL HG-SIL HG-SIL
Onkologie in der ÖGGG): L. Hefler3, P. Kohlberger3, low-grade high-grade high-grade
A. Reinthaller3 (in alphabetischer Reihenfolge) GIL Adenodysplasie AIS
(Adenokarzinom in situ)
HPV-assoziierte Läsionen (mit oder ohne CIN) sollen beschrieben
werden.
1. Einleitung CIN = Cervikale Intraepitheliale Neoplasien; SIL = Squamous Intraepithe-
lial Lesions; GIL = Glandular Intraepithelial Lesions
Die vorliegende Leitlinie zur Diagnose und
Therapie der Cervikalen Intraepithelialen
Neoplasie (CIN) wurde unter besonderer Tabelle 2: Nomenklatur und Klassifikation kolposkopischer Be-
Berücksichtung des Managements suspek- funde, Barcelona 2002, modifizierte deutschsprachige Fassung
ter und pathologischer zytologischer Be-
I. Normale Befunde
funde von den oben angeführten Experten
Originäres Plattenepithel
der AGK und AGO gemeinsam erstellt. Die Zylinderepithel (Ektopie)
Empfehlungen sollen die Abklärung von Normale Transformationszone (Typ 1–3)
auffälligen zytologischen Befunden und de-
ren Therapie in Österreich möglichst ver- II. Abnorme Befunde
einheitlichen. Es wird ausdrücklich ver- Atypische Transformationszone (essigweißes Epithel)
merkt, daß in Österreich die Kolposkopie Zartes Mosaik
Zarte Punktierung
von den Sozialversicherungen honoriert Grobes Mosaik
wird, während die Kosten der HPV-Testung Grobe Punktierung
nur bei entsprechender Indikation über- Atypische Gefäße
nommen werden. Aus forensischen Grün-
III. Verdacht auf invasives Karzinom
den wird geraten, ein Abweichen von der
vorliegenden Leitlinie zu begründen und IV. Ungenügende kolposkopische Beurteilung
zu dokumentieren. Zylinder-Plattenepithelgrenze nicht sichtbar
Schwere Entzündung, schwere Atrophie, Trauma
Portio nicht einstellbar
1
Österreichische Gesellschaft für Zytologie V. Verschiedene kolposkopische Befunde
2
Abteilung für Gynäkologie und Geburtshilfe,
Thermenklinikum Baden Kondylomatöse Läsionen
3
Universitätsklinik für Frauenheilkunde, Keratose
Erosion
Medizinische Universität Wien
4 Polypen
Geburtshilflich-Gynäkologische Universitäts-
Entzündung
klinik, Graz Atrophie
5
Universitätsklinik für Frauenheilkunde, Medi- Deziduose
20 zinische Universität Innsbruck
For personal use only. Not to be reproduced without permission of Krause & Pachernegg GmbH.23. Jahrgang, 3/2005
Tabelle 3: Nomenklatur und zervixzytologische Befundwieder- 2.4. Gewinnung der Histologie: Gewebs-
gabe: Qualität des Abstriches entnahme durch:
A. Beurteilbar
a) beurteilbar und repräsentativ (geschätzt 8–10.000 gut erhaltene I Knipsbiopsie mit Biopsiezange, unter
Plattenepithelzellen, Zylinderepithelzellen und/oder kolposkopischer Sicht am Punctum
Metaplasiezellen) maximum der Veränderung
b) beurteilbar, aber: I Hochfrequenz-Schlingen-Exzision
I keine Zylinderepithel- und/oder Metaplasiezellen
I andere Ursachen (Blut, Entzündung etc.)
(„see and treat“)
I Endozervikale Kürettage (bei Verdacht
B. Nicht beurteilbar (siehe PAP 0)
auf endozervikalen Prozeß)
Gruppe Zytologischer Befund 2.5. Virustypisierung: Eine chronische In-
0 Nicht beurteilbar fektion mit humanen Papillomaviren der
a) nicht bearbeitet wegen technischer/administrativer Hochrisikogruppe (HPV-HR) ist in den mei-
Mängel
b) bearbeitet – aber nicht auswertbar wegen ...
sten Fällen eine notwendige Voraussetzung
I* Normales, altersentsprechendes Zellbild in repräsentativen für die Entwicklung des Zervixkarzinoms
Abstrichen und seiner Vorstufen. Zwischen initialer In-
Leichte Entzündung ohne Epithelalteration fektion und invasivem Karzinom wird in
Metaplasie
den meisten Fällen eine Latenz von mehre-
II* Entzündliche, regenerative, metaplastische oder degenera-
tive Veränderungen ren Jahren angenommen. Daraus ergibt
Normale Endometriumzellen (Angabe postmenopausal sich, daß ein negativer Test auf HPV-HR ei-
obligatorisch) nen hohen negativen Vorhersagewert hat;
Hyper- und Parakeratose das Vorliegen behandlungsbedürftiger zer-
HPV-assoziierte Veränderungen ohne auffällige Kernverän-
derungen
vikaler Dysplasien kann über einen länge-
Atrophisches Zellbild mit Autolyse ren Zeitraum weitgehend ausgeschlossen
III Stärker ausgeprägte entzündliche und/oder degenerative werden.
und/oder atrophe Veränderungen mit nicht sicher
beurteilbarer Dignität (CIN oder invasives Karzinom nicht 2.5.1. Methodik der HPV-HR-Diagnostik
auszuschließen). Das Standardverfahren zum Nachweis von
IIID Zellen einer leichten bis mäßigen Dysplasie (CIN I–II) HPV-HR DNA ist derzeit der Hybrid Cap-
IIIG Auffällige glanduläre Zellen der Endozervix oder des Endo-
metriums (Verdacht auf proliferative oder neoplastische
ture 2 Test (HC-2, Digene, Gaithersburg,
Veränderungen). USA). Der HC-2 Test ist standardisiert, gut
IV Zellen einer mäßigen bis schweren Dysplasie oder eines reproduzierbar und derzeit als einziger
Plattenepithel- oder Adenokarzinoms in situ (CIN II–III, Test von der amerikanischen Gesundheits-
AIS), kein faßbarer Anhaltspunkt für Invasion. behörde Food and Drug Administration
V Zellen eines vermutlich invasiven Plattenepithel- oder
Adenokarzinoms der Zervix oder anderer maligner Tumoren. (FDA) für HPV-HR-Bestimmungen zuge-
lassen.
* Die Gruppen PAP I und II können in eine Gruppe (PAP II) zusammen-
gefaßt werden bei Verzicht auf die Verwendung einer Gruppe PAP I. 2.5.2. Indikationen der HPV-HR-Diagnostik
I Triage beim Pap III: Die kontrolliert-
randomisierte, dreiarmige ALTS-Studie
2. Diagnose mit 3488 Frauen mit Atypical Squamous
Cells of Undetermined Significance
Zur Erkennung von dysplastischen Verän- (ASCUS) ergab für den HC-2 Test einen
derungen an der Portio wird folgender negativen Vorhersagewert von 99 %.
Untersuchungsgang empfohlen. Dies konnte durch weitere Studien be-
stätigt werden. Da die zytologischen Be-
2.1. Inspektion funde PAP III und ASCUS einander nicht
vollständig entsprechen und die Kolpo-
2.2. Kolposkopie: Nativ nach Reinigung skopie in Österreich von den Sozialver-
der Portio, gezielter Zellabstrich, Essig- sicherungsträgern honoriert wird, wur-
probe (3 % Essigsäure), Schiller’sche Jod- de die histologische Abklärung für den
probe, Dokumentation (schriftlich, Zeich- PAP III wie in der Abbildung 1 und Abbil-
nung, Foto, Video). dung 2 empfohlen.
I Follow-up nach Therapie von CIN: Pro-
2.3. Zytologie: Abstrich von der Ekto- und spektive Observationsstudien haben ge-
Endozervix (Transformationszone) mit ge- zeigt, daß der HPV-HR-Nachweis am
eignetem Abnahmegerät (Bürste, Spatel), sensitivsten residuelle oder rezidivie-
sofortige Fixierung mit geeignetem Spray rende CIN anzeigt. Randomisierte Stu-
oder Einstellen in 96 % Alkohol für minde- dien liegen hierfür nicht vor. Der HPV-
stens 10 Minuten. HR-Test kann 6 Monate nach Therapie 2123. Jahrgang, 3/2005
durchgeführt werden. Bei positivem Test- 80 % aller Patientinnen mit Pap III D und
ergebnis und unauffälliger Zytologie, Hi- PAP IV kann eine Infektion mit HPV-HR
stologie und Kolposkopie empfiehlt sich nachgewiesen werden. Aus diesem Grund
ein neuerlicher Test 12 Monate nach der ist die Durchführung des HPV-HR-Tests in
Erstbehandlung. Frauen mit negativem diesen Fällen nicht sinnvoll, da durch den
HPV-HR-Test können in jährlichen Inter- Test keine klinisch relevante Information
vallen weiter kontrolliert werden. Bei über gewonnen werden kann.
3. Management suspekter und pathologischer zytologischer Befunde
3.1. Management von Patientinnen mit PAP III
Aktionsfelder; Ergebnisfelder; HPV: HPV „high risk“; ECC: Endozervi-
Aktionsfelder; Ergebnisfelder
kale Kürettage
1: Management von Patientinnen mit PAP III ohne Atrophie oder Ent- 2: Management von Patientinnen mit PAP III und Vd. auf Atrophie oder
zündung Entzündung
3.2. Management von Patientinnen mit PAP IIIG 3.3. Management von Patientinnen mit PAP IIID
Aktionsfelder;
Ergebnisfelder
3: Management von Patientinnen mit PAP IIIG
Aktionsfelder; Ergebnisfelder; ECC: Endozervikale Kürettage;
4: Management von
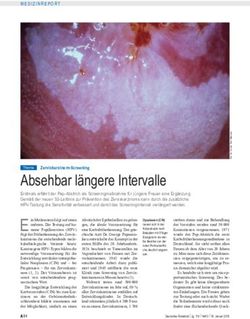
aussagekräftige Kolposkopie: Zylinder-Plattenepithel-Grenze und Läsion
L
Patientinnen mit PAP IIID vollständig einsehbar
2223. Jahrgang, 3/2005
3.4. Management von Patientinnen mit 3.5. Management von Patientinnen mit
PAP IV PAP V
Aktionsfelder; Ergebnisfelder, ECC: Endozervikale Kürettage
6: Management von Patientinnen mit PAP V
L
5: Management von Patientinnen mit PAP IV
Aktionsfelder; Ergebnisfelder; ECC: Endozervikale Kürettage; aussage-
kräftige Kolposkopie: Zylinder-Plattenepithel-Grenze und Läsion vollständig
einsehbar
4. Vorgangsweise bei histologisch verifizierter CIN I, CIN II, CIN III
4.2. Oberflächendestruktion
Mögliche Indikationen:
I koilozytäre Läsion ohne CIN
I CIN I, LG-SIL
Voraussetzungen:
I ektozervikal gelegen,
I vollständig einsehbar
I nach vorangegangener Biopsie
I kolposkopische und zytologische
Kontrolle in 6 Monaten gesichert
Aktionsfelder; Ergebnisfelder
7: Management von Patientinnen mit CIN I–III
4.3. Weiteres Vorgehen nach Konisation
4.1. Resektion I CIN im Gesunden entfernt: Gynäkologi-
sche Kontrollen (Kolposkopie, Zytolo-
Indikationen: gie) in Routineintervallen; der HPV-HR-
I persistierende CIN I, LG-SIL Test kann 6 Monate nach Therapie
I CIN II, CIN III, HG-SIL, rezidivierende durchgeführt werden. Bei positivem
pathologische Zytologie ohne histologi- Testergebnis und unauffälliger Zytolo-
sches Korrelat gie, Histologie und Kolposkopie emp-
I Verdacht auf Frühinvasion fiehlt sich eine neuerliche HPV-HR-Te-
I Verdacht auf glanduläre intraepitheliale stung 12 Monate nach der Erstbe-
Läsion handlung. Frauen mit negativem HPV-
HR-Test können in jährlichen Interval-
Technik: len weiter kontrolliert werden.
I Konisation mittels Hochfrequenz-Schlin-
ge (LEEP, Loop-excision, Loop conebiop- I CIN I, CIN II, CIN III nicht im Gesunden
sy; LLETZ) oder Skalpell (Messerkoni- (non in sano) entfernt: Siehe Abbildung
sation) 8 und 9 2323. Jahrgang, 3/2005
Aktionsfelder; Ergebnisfelder; HPV: HPV „high risk“
8: Konisation ektozervikal non in sano
Aktionsfelder; Ergebnisfelder; HPV: HPV „high risk“; ECC: Endo-
zervikale Kürettage
9: Konisation endozervikal non in sano
5. Mikrokarzinom (Früh-/Mikro- 6. CIN in der Schwangerschaft
invasives Karzinom) der Cervix
uteri 6.1. Diagnose
I Kolposkopie
5.1. Stadieneinteilung: nach der
FIGO Klassifikation 1994 I Zytologie
5.2. Diagnose nur histologisch, nach I histologische Abklärung bei Verdacht
Konisation: auf Invasion
I Stadium Ia1: Oberflächenausdehnung
≤ 7 mm, Tiefenwachstum ≤ 3 mm 6.2. Therapie
I Stadium Ia2: Oberflächenausdehnung
≤ 7 mm, Tiefenwachstum > 3 mm, aber 6–8 Wochen post partum, siehe die ent-
≤ 5 mm. sprechenden Abbildungen
Ein allfälliger Gefäßeinbruch bedingt keine
Änderung der Stadieneinteilung, muß aber
vom Pathologen vermerkt werden.
5.3. Therapie (siehe auch Leitlinie der AGO:
Gynäkol Geburtshilfliche Rundschau 1997;
37: 227–9)
I Stadium Ia1, in sano, kein Gefäßeinbruch:
keine weitere Therapie
I Stadium Ia1, mit Gefäßeinbruch: pelvine
Lymphadenektomie
I Stadium Ia2, mit und ohne Gefäßein-
bruch: pelvine Lymphadenektomie, der
Wunsch nach Erhaltung der Fertilität
bestimmt die Indikation zur Hysterekto-
mie.
2423. Jahrgang, 3/2005
LITERATUR: Stoler MH, Schiffman M. Interobserver reproduc-
ibility of cervical cytologic and histologic interpre-
Bar-Am A, Gamzu R, Levin I et al. Follow-up by tations: realistic estimates from the ASCUS-LSIL
combined cytology and human papillomavirus Trial Study. JAMA 2001; 285: 1500–5.
testing for patients post-cone biopsy: results of a Schneider A, Hoyer H, Lotz B et al. Screening for
long term follow-up. Gynecol Oncol 2003; 91: 149– high-grade cervical intraepithelial neoplasia and
53. cancer by testing for high-risk HPV, routine cytol-
Böhmer G, van den Brule AJ, Brummer O et al. No ogy or colposcopy. Int J Cancer 2000; 89: 529–34.
confirmed case of human papillomavirus DNA Solomon D, Schiffman M, Tarone R. Comparision
negative cervical intraepithelial neoplasia grade III of three management strategies for patients with
(CIN III) or invasive primary cancer of the uterine atypical squamous cells of undetermined signifi-
cervix among 511 patients. Am J Obstet Gynecol cance: baseline results from a randomized trial. J
2003; 189: 118–20. Natl Cancer Inst 2001; 93: 293–9.
Bosch FX, Lorincz A, Munoz N et al. The causal re- Walboomers JM, Jacobs MV, Manos MM et al. Hu-
lation between human papillomavirus and cervical man papillomavirus is a necessary cause of invasive
cancer. J Clin Pathol 2002; 55: 244–65. cervical cancer worldwide. J Pathol 1999; 189: 12–
Girardi F, Pickel H, Joura EA et al. Guidelines for 9.
diagnosis and therapy of intraepithelial neoplasia Wells M, Östör AG, Crum CP et al. Tumors of the
and early invasive carcinoma of the female lower cervix, epithelial tumors. In: Tavassoli FA (ed).
genital system (cervix uteri, vagina, vulva) estab- WHO classification of tumors, pathology & genet-
lished by the AGK (Colposcopy Work Group in the ics, Tumors of the breast and female genital organs.
OGGG [Austrian Society of Gynecology and Obstet- WHO, IARC Press, Lyon, France, 2003.
rics]). Gynakol Geburtshilfliche Rundsch 2001; 41: Winter R, Concin H, Fuith L et al. Guidelines for
197–200. surgical treatment of cervix carcinoma developed
Houfflin-Debarge V, Collinet P, Vinatier D et al. by the Standard Committee of the Austrian Society
Value of papillomavirus testing after conization by of Gynecology and Obstetrics. Austrian Society of
loop electrosurgical excision for high-grade squa- Gynecology and Obstetrics. Gynakol Geburtshilf-
mous intraepithelial lesions. Gynecol Oncol 2003; liche Rundsch 1997; 37: 227–9.
90: 587–92. Wright TC Jr, Cox JT, Massad LS et al. ASCCP-Spon-
Modifications in the staging for stage I vulvar and sored Consensus Conference 2001 Consensus
stage I cervical cancer. Report of the FIGO Com- Guidelines for the management of women with cer-
mittee on Gynecologic Oncology. International vical cytological abnormalities. JAMA 2002; 287:
Federation of Gynecology and Obstetrics. Int J 2120–9.
Gynaecol Obstet 1995; 50: 215–6. Zielinski GD, Rozendaal L, Voorhorst FJ et al. HPV
Parker MF, Zahn CM, Vogel KM et al. Discrepancy testing can reduce the number of follow-up visits in
in the interpretation of cervical histology by women treated for cervical intraepithelial neopla-
gynecologic pathologists. Obstet Gynecol 2002; sia grade 3. Gynecol Oncol 2003; 91: 67–73.
100: 277–80. Zauna RE, Sienko A, Lightfoot S et al. Cervical
Petry KU, Menton S, Menton M et al. Inclusion of smear interpretations in women with histologic di-
HPV testing in routine cervical cancer screening agnosis of severe dysplasia: factors associated with
for women above 29 years in Germany: results from discrepant interpretations. Cancer 2002; 96: 218–
8466 patients. Br J Cancer 2003; 88: 1570–7. 24.
25Mitteilungen aus der Redaktion
Abo-Aktion
Wenn Sie Arzt sind, in Ausbildung zu einem ärztlichen Beruf, oder im Gesundheitsbereich tätig,
haben Sie die Möglichkeit, die elektronische Ausgabe dieser Zeitschrift kostenlos zu beziehen.
Die Lieferung umfasst 4–6 Ausgaben pro Jahr zzgl. allfälliger Sonderhefte.
Das e-Journal steht als PDF-Datei (ca. 5–10 MB) zur Verfügung und ist auf den meisten der
marktüblichen e-Book-Readern, Tablets sowie auf iPad funktionsfähig.
Bestellung kostenloses e-Journal-Abo
Besuchen Sie unsere
zeitschriftenübergreifende Datenbank
Bilddatenbank Artikeldatenbank Fallberichte
Haftungsausschluss
Die in unseren Webseiten publizierten Informationen richten sich ausschließlich an geprüfte
und autorisierte medizinische Berufsgruppen und entbinden nicht von der ärztlichen Sorg-
faltspflicht sowie von einer ausführlichen Patientenaufklärung über therapeutische Optionen
und deren Wirkungen bzw. Nebenwirkungen. Die entsprechenden Angaben werden von den
Autoren mit der größten Sorgfalt recherchiert und zusammengestellt. Die angegebenen Do-
sierungen sind im Einzelfall anhand der Fachinformationen zu überprüfen. Weder die Autoren,
noch die tragenden Gesellschaften noch der Verlag übernehmen irgendwelche Haftungsan-
sprüche.
Bitte beachten Sie auch diese Seiten:
Impressum Disclaimers & Copyright DatenschutzerklärungSie können auch lesen